Το μαγνήσιο (Mg) εμπλέκεται στη ρύθμιση του μεταβολισμού και στη διατήρηση της ομοιόστασης όλων των ιστών, συμπεριλαμβανομένου του εγκεφάλου, όπου εναρμονίζει
τη μετάδοση του νευρικού σήματος και διατηρεί την ακεραιότητα του αιματοεγκεφαλικού φραγμού.
 |
|
Δρ Δημήτριος Ν. Γκέλης Ιατρός, Ωτορινολαρυγγολόγος, Οδοντίατρος, Διδάκτωρ της Ιατρικής Σχολής του Πανεπιστημίου Αθηνών
Kόρινθος 20100 pharmage@otenet.gr gelis.gr pharmagel.gr Τηλ. 6944280764
|
 |
| Αικατερίνη Γκέλη Ιατρός, Ακτινοδιαγνώστρια Παπαληγούρα 16 Άσσος Κορινθίας 6944644820 |
Η έλλειψη Mg συμβάλλει στη δημιουργία συστηματικής φλεγμονής χαμηλού βαθμού, τον κοινό παρονομαστή των περισσότερων ασθενειών. Ειδικότερα, η νευροφλεγμονή είναι το χαρακτηριστικό των νευροεκφυλιστικών διαταραχών.
Στην παρουσα σύντομη ανασκόπηση περιγράφεται ο ρόλος του μαγνησίου στον εγκέφαλο και παρέχονται στοιχεία που συνδέουν τη διαταραχή της ισορροπίας του μαγνησίου με τη σκλήρυνση κατά πλάκας, αλλά και με άλλες νευροεκφυλιστικές νόσους, όπως η νόσος του Αλτσχάιμερ και η νόσος του Πάρκινσον[1].
O ρόλος του μαγνησίου στον εγκέφαλο
Έχει παρατηρηθεί σε αρουραίους πειραματόζωα ότι, η αύξηση του μαγνησίου του εγκεφάλου οδηγεί στην ενίσχυση των μαθησιακών ικανοτήτων, της μνήμης εργασίας και της βραχυπρόθεσμης και μακροπρόθεσμης μνήμης[2].
Από νευρολογικής άποψης, το μαγνήσιο παίζει ουσιαστικό ρόλο στη νευρική μεταβίβαση και τη νευρομυϊκή αγωγιμότητα. Λειτουργεί επίσης προστατευτικά έναντι της υπερβολικής διέγερσης που μπορεί να οδηγήσει σε θάνατο νευρωνικών κυττάρων (διεγερτοτοξικότητα) και έχει εμπλακεί σε πολλαπλές νευρολογικές διαταραχές[3].
Το Mg είναι ένα ζωτικής σημασίας ιχνοστοιχείο με ουσιαστικούς ρόλους στον ενεργειακό μεταβολισμό, την ομοιόσταση του ασβεστίου, την ενζυματική δραστηριότητα και τη διακυτταρική μεταφορά.
Στον εγκέφαλο, το Mg διεγείρει τους υποδοχείς του γ-αμινοβουτυρικού οξέος (GABA-Rs) και αναστέλλει τον υποδοχέα N-μεθυλ-D-ασπαρτικού (NMDA-R) [4].
Σταθεροποιεί τον αιματεγκεφαλικό φραγμό (BBB) [5], ρυθμίζει τον άξονα των επινεφριδίων και της υποθαλαμικής υπόφυσης [6] και συμμετέχει στη ρύθμιση της μεταγραφής των γονιδίων που εμπλέκονται στη νευροδιαβίβαση [7].
Το Mg έχει επίσης ρόλο στη ρύθμιση της απελευθέρωσης νευροπεπτιδίων και στην εξουδετέρωση του οξειδωτικού στρες, συμβάλλοντας έτσι στη διατήρηση της υγιούς νευρολογικής λειτουργίας [8, 9].
Η ανισορροπία της ομοιόστασης Mg έχει συσχετιστεί με νευρολογικές ασθένειες και ψυχιατρικές διαταραχές [4].
Το Mg ανταγωνίζεται το NMDA-R, του οποίου η υπερενεργοποίηση συνδέεται με νευρωνική βλάβη σε αρκετές οξείες και χρόνιες διαταραχές, συμπεριλαμβανομένων των νόσων Alzheimer και Huntington, εγκεφαλικού επεισοδίου και τραυματικού εγκεφαλικού τραυματισμού [10] .
Ενώ απαιτείται περισσότερη έρευνα για το Mg ως συμπληρωματικής θεραπείας στη νόσο του Αλτσχάιμερ και του Πάρκινσον, τα αναδυόμενα δεδομένα υποστηρίζουν την προστατευτική δράση του Mg σε εγκεφαλικά επεισόδια και τραυματικές βλάβες του εγκεφάλου [4]. Επίσης η χορήγηση Mg συνιστάται για την πρόληψη των κρίσεων που σχετίζονται με την προεκλαμψία στις εγκύους[4] .
Το Mg βελτιώνει το άγχος και το στρες ενεργοποιώντας το GABAεργικό μονοπάτι [11].
Το γ-αμινοβουτυρικό οξύ (GABA) είναι ο κύριος ανασταλτικός νευροδιαβιβαστής στο κεντρικό νευρικό σύστημα και δρα μέσω των ιοντοτροπικών υποδοχέων GABA τύπου Α (GABA A ) και μεταβοτροπικών GABA τύπου Β (GABA B). Μόλις το GABA δεσμεύσει τους υποδοχείς του, γίνονται διαπερατοί στην εισροή χλωρίου, η οποία καταστέλλει τη νευρωνική δραστηριότητα στον εγκέφαλο [12].
Η δυσλειτουργία αυτών των GABA-R σχετίζεται με άγχος, επιληψία και νευροαναπτυξιακές διαταραχές, συμπεριλαμβανομένου του αυτισμού [13]. Είναι σημαντικό ότι η ανεπάρκεια των υποδοχέων GABA A έχει ως αποτέλεσμα την υπερδραστηριότητα του NMDA-R και, ως εκ τούτου, την πρόκληση διεγερτικής τοξικότητας [14].
Το γλουταμινικό οξύ μέσω NMDA-R και το GABA μέσω του GABA A -R έχει αποδειχθεί ότι ρυθμίζει προς τα πάνω τον νευροτροφικό παράγοντα που προέρχεται από τον εγκέφαλο (BDNF) στους νευρώνες του ιππόκαμπου και του υποθαλάμου [15]. Ο BDNF είναι μια νευροτροφίνη που εμπλέκεται στην ανάπτυξη και διατήρηση του νευρικού συστήματος [16] και συντίθεται όχι μόνο από νευρώνες, αλλά και από το εγκεφαλικό ενδοθήλιο. Ο BDNF που προέρχεται από το ενδοθήλιο προστατεύει τους νευρώνες από το οξειδωτικό στρες, την υποξία και την τοξικότητα του αμυλοειδούς [17]. Αντίστοιχα, το ανθυγιεινό εγκεφαλικό ενδοθήλιο σχετίζεται με νευρωνική δυσλειτουργία [18].
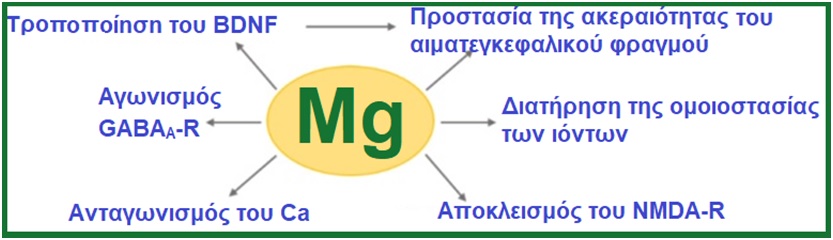
Ο ρόλος του μαγνησίου στον εγκέφαλο. Το μαγνήσιο στον εγκέφαλο παίζει θεμελιώδη ρόλο στη διαμόρφωση διαφορετικών βιοχημικών οδών[1].
H σχέση του μαγνησίου και της νευροφλεγμονής
Το μαγνήσιο, μεταξύ των άλλων δράσεών του ρυθμίζει επίσης τις ανοσολογικές λειτουργίες, δρώντας στα κύτταρα του έμφυτου και προσαρμοστικού ανοσοποιητικού συστήματος. Η έλλειψη μαγνησίου ενεργοποιεί τα φαγοκύτταρα, ενισχύει την οξειδωτική έκρηξη των κοκκιοκυττάρων, ενεργοποιεί τα ενδοθηλιακά κύτταρα και αυξάνει τα επίπεδα των κυτοκινών, προάγοντας έτσι τη φλεγμονή. Κατά συνέπεια, μια χαμηλή κατάσταση μαγνησίου, η οποία συχνά υποδιαγιγνώσκεται, ενισχύει την αντιδραστικότητα σε διάφορες προκλήσεις του ανοσοποιητικού και εμπλέκεται στην παθοφυσιολογία πολλών συνηθισμένων χρόνιων ασθενειών[1].
Η νευροφλεγμονή οδηγεί σε βλάβη των ιστών σε νευροεκφυλισμό. Συμπαγή δεδομένα υποδηλώνουν ένα ρόλο του Mg στην εξασθένιση της νευροφλεγμονής και στην επιβράδυνση ορισμένων νευροεκφυλιστικών ασθενειών. Επομένως, μια σωστή και, ει δυνατόν, εξατομικευμένη διατροφική πρόσληψη Mg μπορεί να αποτελεί προληπτικό μέτρο, ενώ η συμπλήρωση Mg μπορεί να είναι μια συμπληρωματική επιλογή στον νευροεκφυλισμό[1].
Οι επιπτώσεις του χαμηλού μαγνησίου στον εγκέφαλο. Η έλλειψη μαγνησίου είναι υπεύθυνη για την αύξηση της νευροφλεγμονής και τη δυσλειτουργία του Αιματεγκεφαλικού φραγμού[1].
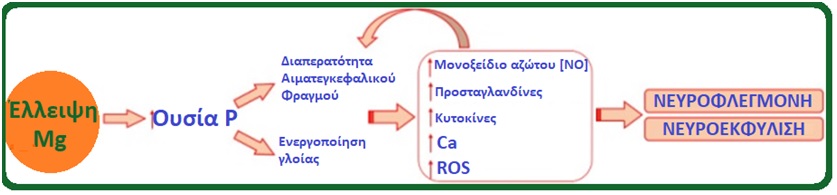
Οι επιπτώσεις του χαμηλού μαγνησίου στον εγκέφαλο. Η έλλειψη μαγνησίου είναι υπεύθυνη για την αύξηση της νευροφλεγμονής και τη δυσλειτουργία του Αιματεγκεφαλικού φραγμού[1].
Η σχέση της σκλήρυνσης κατά πλάκας και της έλλειψης μαγνησίου
Η σκλήρυνση κατά πλάκας (ΣΚΠ) είναι μια επίκτητη νευρολογική ασθένεια η οποία προκαλεί αναπηρία σε νεαρά ενήλικα άτομα και επηρεάζει περίπου 2,3 εκατομμύρια ανθρώπους παγκοσμίως. Είναι πιο διαδεδομένη στη Βόρεια Αμερική (140 περιπτώσεις ανά 100.000) και στην Ευρώπη (108 περιπτώσεις ανά 100.000). Ο επιπολασμός είναι χαμηλότερος στην υποσαχάρια Αφρική (2,1 περιπτώσεις ανά 100.000) και στην Ανατολική Ασία (2,2 περιπτώσεις ανά 100.000)[19].
Η σκλήρυνση κατά πλάκας είναι μια φλεγμονώδης νόσος του κεντρικού νευρικού συστήματος (ΚΝΣ), η οποία προκαλεί μια ετερογενή σειρά συμπτωμάτων και σημείων λόγω της διαφορικής συμμετοχής κινητικών, αισθητηριακών, οπτικών και αυτόνομων συστημάτων. Η οπτική νευρίτιδα (φλεγμονή του οπτικού νεύρου), το φαινόμενο Uhthoff (παροδική διακύμανση ή επιδείνωση των συμπτωμάτων ΣΚΠ με αύξηση της θερμοκρασίας του σώματος) και το φαινόμενο Lhermitte (μια μη φυσιολογική αίσθηση ηλεκτροπληξίας στη σπονδυλική στήλη ή τα άκρα στην κάμψη του αυχένα) είναι χαρακτηριστικά της νόσου [20] και συμβαίνουν λόγω των εστιακών περιοχών απομυελίνωσης που εξελίσσονται σε 24 ώρες και επιμένουν για μέρες ή εβδομάδες πριν γενικά, αν και όχι αποκλειστικά, βελτιωθούν[21, 22].
Η μαγνητική τομογραφία (MRI) είναι ένα βασικό συμπληρωματικό κλινικό εργαλείο όσον αφορά τη διάγνωση και τη θεραπευτική παρακολούθηση.
Χαρακτηριστικά της σκλήρυνσης κατά πλάκας είναι η απομυελίνωση και η αξονική εκφύλιση σε διάφορες περιοχές του εγκεφάλου και του νωτιαίου μυελού, καθώς και η διαταραχή του αιματεγκεφαλικού φραγμού, συμβάντα που προκαλούνται από την ενεργοποίηση της φλεγμονής [23].
Οι κυτοκίνες, το μονοξείδιο του αζώτου (ΝΟ) και η δυσλειτουργία των μιτοχονδρίων είναι κύριοι καθοριστικοί παράγοντες για την έναρξη, την υποτροπή και την εξέλιξη της νόσου. Λαμβάνοντας υπόψη την αντιφλεγμονώδη δράση του Mg και τον ρόλο του στη διατήρηση της μιτοχονδριακής λειτουργίας, ο πιθανός προστατευτικός ρόλος μιας σωστής πρόσληψης Mg είναι εφικτός.
Η απορρύθμιση του ανοσοποιητικού μονοπατιού είναι ένα από τα κοινά χαρακτηριστικά του νευροεκφυλισμού. Πρόσφατα, υπάρχει αυξανόμενο ενδιαφέρον για τον ειδικό ρόλο των Τ βοηθητικών κυττάρων Th 17 και της Ιντερλευκίνης-17Α (IL-17A), της πιο σημαντικής κυτοκίνης των κυττάρων Th 17, στην παθογένεση νευροεκφυλιστικών ασθενειών του κεντρικού νευρικού συστήματος (ΚΝΣ) . Όπως και στη νόσο του Αλτσχάιμερ, τα Th17 κύτταρα είναι τα δραστικά κύτταρα κλειδιά και βασικοί τελεστές στη σκλήρυνση κατά πλάκας και κατά συνέπεια, η IL17 εκφράζεται σε μεγάλο βαθμό στον εγκέφαλο των ασθενών [24].
Ο TRPM7 (Transient Receptor Potential Cation Channel Subfamily M Member 7) υπερεκφράζεται σε αστροκύτταρα που έχουν απομονωθεί από ασθενείς με σκλήρυνση κατά πλάκας και αυτή η απορρύθμιση φαίνεται να εμπλέκεται στα πρώιμα και στα τελευταία στάδια της σκλήρυνσης κατά πλάκας. Αρχικά, το ρυθμισμένο προς τα πάνω TRPM7 μπορεί να οδηγήσει στη συσσώρευση λεμφοκυττάρων Th17, ευνοώντας έτσι τη φλεγμονή [25].
Στη συνέχεια, μπορεί να ευνοήσει την εξέλιξη της νόσου επειδή η υπερέκφραση του TRPM7 συνδέεται με το σχηματισμό των γλοιωτικών ουλών [26].
Επιπλέον, λόγω της ανταγωνιστικής του δράσης στο Ca, η συμπληρωματική χορήγηση μαγνησίου βελτίωσε τη σοβαρή σπαστική παραπληγία σε νεαρό ασθενή με σκλήρυνση κατά πλάκας [27].
Σχέση του μαγνησίου, της βιταμίνης D3 και της σκλήρυνσης κατά πλάκας
Με βάση τις επιδημιολογικές μελέτες, ~75% όλων των ενηλίκων παγκοσμίως έχουν επίπεδα 25(OH)D στον ορό <30 ng/mL, δηλαδή βρισκόμαστε ενώπιον μιας πανδημίας έλλειψης ή ανεπάρκειας βιταμίνης D. Λόγω της πρόσφατης αύξησης της παγκόσμιας ευαισθητοποίησης γιαυτό το θέμα, η λήψη συμπληρωμάτων βιταμίνης D3 έχει γίνει κοινή πρακτική, αλλά η έλλειψη Mg εξακολουθεί να παραμένει αδιευκρίνιστη. Ο έλεγχος για χρόνια ανεπάρκεια μαγνησίου είναι δύσκολος επειδή ένα φυσιολογικό επίπεδο στον ορό μπορεί να εξακολουθεί να σχετίζεται με μέτρια έως σοβαρή ανεπάρκεια. Μέχρι σήμερα, δεν υπάρχει απλή και ακριβής εργαστηριακή εξέταση για τον προσδιορισμό της συνολικής κατάστασης του μαγνησίου του σώματος στον άνθρωπο. Άλλωστε οι μετρήσεις του μαγνησίου του ορού μπορεί να βρεθούν εντός των φυσιολογικών ορίων, αλλά να υπάρχει έλλειψη στο ενδοκυττάριο μαγνήσιο. Όμως, το Mg είναι απαραίτητο στο μεταβολισμό της βιταμίνης D και η λήψη μεγάλων δόσεων βιταμίνης D μπορεί να προκαλέσει σοβαρή μείωση του Mg.
Επιπλέον, δεδομένου ότι η έλλειψη της βιταμίνης D3 φαίνεται να παίζει αιτιολογικό ρόλο στη νόσο, αξίζει να σημειωθεί ότι το Mg απαιτείται για το μεταβολισμό της βιταμίνης D3. Συνεπώς συνιστάται να χορηγείται στους πάσχοντες με έλλειψη βιταμίνης D3 ή σε όσους πάσχοντες εφαρμόζονται θεραπευτικά πρωτόκολλο χορήγησης μεγάλων δόσεων βιταμίνης D3, η συμπληρωματική χορήγηση μαγνησίου [28].
Σταδιακά εμφανίζονται στη βιβλιογραφία περισσότερα δεδομένα, που υποδηλώνουν ότι η 1,25-διυδροξυβιταμίνη D3 ή η 1,25(OH)2D3, δηλαδή η δραστική βιταμίνη D3, καταστέλλει τη διαφοροποίηση των δυνητικά παθογόνων Τ κυττάρων που σχετίζονται με τη ΣΚΠ, ενισχύει τη διαφοροποίηση των ρυθμιστικών Τ κυττάρων, που καταστέλλουν τα παθογόνα Τ κύτταρα και προάγει την επαναμυελίνωση. Οι λειτουργίες της βιταμίνης D3 έχουν ενθαρρύνει τους ερευνητές να αναπτύξουν τη βιταμίνη D3 ως πιθανή θεραπεία για τη σκλήρυνση κατά πλάκας. Μια ομάδα νεαρών ασθενών με σκλήρυνση κατά πλάκας υποβλήθηκε σε θεραπεία με συμπληρώματα διατροφής που περιείχαν ασβέστιο, μαγνήσιο και βιταμίνη D3 για περίοδο ενός έως δύο ετών. Ο πειραματικός σχεδιασμός χρησιμοποίησε αυτο-σύζευξη, δηλαδή, η ανταπόκριση κάθε ασθενή συγκρίθηκε με το δικό του ιστορικό περιπτώσεων ως μάρτυρα. Ο αριθμός των παροξύνσεων που παρατηρήθηκαν κατά τη διάρκεια του προγράμματος ήταν μικρότερος από το μισό του αριθμού που αναμενόταν από τα ιστορικά περιστατικών. Δεν υπήρξαν εμφανείς παρενέργειες. Αυτό το συμπληρωματικό διατροφικό σχήμα μπορεί να προσφέρει ένα νέο μέσο ελέγχου του ποσοστού παροξύνσεων της ΣΚΠ, τουλάχιστον για νεότερους ασθενείς. Τα αποτελέσματα τείνουν να υποστηρίζουν μια θεωρία της ΣΚΠ που δηλώνει ότι το ασβέστιο και το μαγνήσιο είναι σημαντικά για την ανάπτυξη, τη δομή και τη σταθερότητα της μυελίνης[29].
H επίδραση των συγκεντρώσεων του μαγνησίου στον ορό του αίματος μελετήθηκε σε 101 ενήλικα άτομα με διαγνωσμένη υποτροπιάζουσα διαλείπουσα ΣΚΠ από την Karpińska E. και τους συνεργάτες (2017) . Όλοι οι συμμετέχοντες ερευνήθηκαν στην κλίμακα διευρυμένης κατάστασης αναπηρίας. Η ομάδα ελέγχου περιελάμβανε 41 άτομα. Η συγκέντρωση του Mg στον ορό προσδιορίστηκε με τη μέθοδο φασματομετρίας ατομικής απορρόφησης φλόγας.
Οι ασθενείς συμπλήρωσαν μια έρευνα και μια 24ωρη διατροφική συνέντευξη. Σε ασθενείς με ΣΚΠ η μελέτη απέδειξε ότι, οι ασθενείς με φυσιολογικά επίπεδα συγκέντρωσης Mg στον ορό ήταν σε καλύτερη κλινική κατάσταση, ιδιαίτερα όσον αφορά τη λειτουργία της πυραμιδικής οδού ( p = 0,007) και των σφιγκτήρων ( p = 0,002),συγκριτικά προς τους ασθενείς με ανεπαρκή επίπεδα Mg στον ορό. Εξωτερικοί παράγοντες όπως το φύλο, το κάπνισμα, τα ανοσοτροποποιητικά φάρμακα ή τα συμπληρώματα διατροφής Mg βρέθηκε ότι δεν έχουν καμία επίδραση στη συγκέντρωση του Mg στον ορό ασθενών με ΣΚΠ. Τα αποτελέσματα αυτής της μελέτης υποδηλώνουν ότι μια μη φυσιολογική συγκέντρωση Mg στον ορό ασθενών με ΣΚΠ θα πρέπει να αναγνωρίζεται και να διορθώνεται, καθώς αυτό μπορεί να βελτιώσει την κατάσταση της υγείας των ατόμων με ΣΚΠ[30].
Μια άλλη έρευνα ασθενών με σκλήρυνση κατά πλάκας έδειξε μειωμένες συγκεντρώσεις στον ορό τους αρκετών μετάλλων, μεταξύ των οποίων ήταν το Mg, στο αίμα [31].
 Ωστόσο, σύμφωνα με μια πρόσφατη μετανάλυση, δεν προέκυψαν σημαντικές διαφορές μαγνησιαιμίας μεταξύ ασθενών με σκλήρυνση κατά πλάκας και υγιών μαρτύρων [32].
Ωστόσο, σύμφωνα με μια πρόσφατη μετανάλυση, δεν προέκυψαν σημαντικές διαφορές μαγνησιαιμίας μεταξύ ασθενών με σκλήρυνση κατά πλάκας και υγιών μαρτύρων [32].
Σε περίπτωση συμπληρωματικής χορήγησης βιταμίνης D3 και μαγνησίου σε ασθενείς με σκλήρυνση κατά πλάκας επιλέγεται η χορήγηση φυσικής βιταμίνης D3 σε βιολογικό εξαιρετικό παρθένο ελαιόλαδο, χωρίς χημικά συντηρητικά ή άλλα έκδοχα [D3 Gkelin drops].
Δεν συνιστάται η εβδομαδιαία μαζική χορήγηση βιταμίνης D3, διότι δεν απορροφάται ασφαλώς. Αν χορηγηθεί και μαγνήσιο επιλέγεται το Magnigkel, του οποίου κάθε κάψουλα περιέχει 28,5 mg Tαυρικού Mαγνησίου και 143 mg Κιτρικού μαγνησίου, τα οποία διαπερνούν τον αιματεγκεφαλικό φραγμό. Χορηγείται μία κάψουλα Magnigkel πρωί και βράδυ με το φαγητό, ενώ το D3 Gkelin drops χορηγείται το μεσημέρι με το φαγητό. Συνιστάται η αποφυγή χρησιμοποίησης καψουλών που περιέχουν βιταμίνη D3 και μαγνήσιο ταυτόχρονα στην ίδια κάψουλα, διότι είναι αβέβαιη η απορροφητικότητα του καθ΄ενός συστατικού από το λεπτό έντερο. Η δοσολογία της βιταμίνης D3 [D3 Gkelin drops] καθορίζεται από τον θεράποντα νευρολόγο. To D3 Gkelin drops περιέχει 110 σταγόνες.
αιματεγκεφαλικό φραγμό. Χορηγείται μία κάψουλα Magnigkel πρωί και βράδυ με το φαγητό, ενώ το D3 Gkelin drops χορηγείται το μεσημέρι με το φαγητό. Συνιστάται η αποφυγή χρησιμοποίησης καψουλών που περιέχουν βιταμίνη D3 και μαγνήσιο ταυτόχρονα στην ίδια κάψουλα, διότι είναι αβέβαιη η απορροφητικότητα του καθ΄ενός συστατικού από το λεπτό έντερο. Η δοσολογία της βιταμίνης D3 [D3 Gkelin drops] καθορίζεται από τον θεράποντα νευρολόγο. To D3 Gkelin drops περιέχει 110 σταγόνες.
Βιβλιογραφική Τεκμηρίωση
1.Jeanette A. M. Maier, Laura Locatelli, Giorgia Fedele, Alessandra Cazzaniga, and André Mazur/ Magnesium and the Brain: A Focus on Neuroinflammation and Neurodegeneration.Int J Mol Sci. 2023 Jan; 24(1): 223.
2.Slutsky I, Abumaria N, Wu LJ, Huang C, Zhang L, Li B, Zhao X, Govindarajan A, Zhao MG, Zhuo M, Tonegawa S, Liu G. Enhancement of learning and memory by elevating brain magnesium. Neuron. 2010 Jan 28;65(2):165-77
3.Kirkland AE, Sarlo GL, Holton KF. The Role of Magnesium in Neurological Disorders. Nutrients. 2018 Jun 6;10(6):730.
4.Kirkland A.E., Sarlo G.L., Holton K.F. The role of magnesium in neurological disorders. Nutrients. 2018;10:730.
5.Romeo V., Cazzaniga A., Maier J.A.M. Magnesium and the blood-brain barrier in vitro: Effects on permeability and magnesium transport. Magnes. Res. 2019;32:16–24.
6.Boyle N.B., Lawton C., Dye L. The effects of magnesium supplementation on subjective anxiety and stress—A systematic review. Nutrients. 2017;9:429.
7.Dabbah-Assadi F., Khatib N., Ginsberg Y., Weiner Z., Shamir A., Beloosesky R. Short-Term Effect of MgSO4 on the Expression of NRG-ErbB, Dopamine, GABA, and Glutamate Systems in the Fetal Rat Brain. J. Mol. Neurosci. 2021;71:446–454.
8.Fiorentini D., Cappadone C., Farruggia G., Prata C. Magnesium: Biochemistry, Nutrition, Detection, and Social Impact of Diseases Linked to Its Deficiency. Nutrients. 2021;13:1136.
9.Zheltova A.A., Kharitonova M.V., Iezhitsa I.N., Spasov A.A. Magnesium deficiency and oxidative stress: An update. BioMedicine. 2016;6:20.
10.Li V., Wang Y.T. Molecular mechanisms of NMDA receptor-mediated excitotoxicity: Implications for neuroprotective therapeutics for stroke. Neural Regen. Res. 2016;11:1752–1753.
11.Boyle N.B., Lawton C., Dye L. The effects of magnesium supplementation on subjective anxiety and stress—A systematic review. Nutrients. 2017;9:429.
12.Gonzalez-Nunez V. Role of gabra2, GABAA receptor alpha-2 subunit, in CNS development. Biochem. Biophys. Rep. 2015;3:190–201.
13.Zhu S., Noviello C.M., Teng J., Walsh R.M., Kim J.J., Hibbs R.E. Structure of a human synaptic GABAA receptor. Nature. 2018;559:67–88.
14.Sarawagi A., Soni N.D., Patel A.B. Glutamate and GABA Homeostasis and Neurometabolism in Major Depressive Disorder. Front. Psychiatry. 2021;12:419.
15.Marmigère F., Rage F., Tapia-Arancibia L. GABA-glutamate interaction in the control of BDNF expression in hypothalamic neurons. Neurochem. Int. 2003;42:353–358.
16.Cohen-Cory S., Kidane A.H., Shirkey N.J., Marshak S. Brain-derived neurotrophic factor and the development of structural neuronal connectivity. Dev. Neurobiol. 2010;70:271–288.
17.Guo S., Kim W.J., Lok J., Lee S.-R., Besancon E., Luo B.-H., Stins M.F., Wang X., Dedhar S., Lo E.H. Neuroprotection via matrix-trophic coupling between cerebral endothelial cells and neurons. Proc. Natl. Acad. Sci. USA. 2008;105:7582–7587.
18.Wang F., Cao Y., Ma L., Pei H., Rausch W.D., Li H. Dysfunction of Cerebrovascular Endothelial Cells: Prelude to Vascular Dementia. Front. Aging Neurosci. 2018;10:376.
19.Multiple Sclerosis International Federation . London: MSIF; 2013. Atlas of MS mapping multiple sclerosis around the world. 2013.
20.Stevenson EV. Alexander JS. Yun JW. Becker F. Gonzalez-Toledo E. Chapter 16 – Mechanisms of blood–brain barrier disintegration in the pathophysiology of multiple sclerosis. In: Minagar A, editor. Multiple sclerosis. London: Academic Press; 2016. pp. 393–413.
21.Deangelis TM. Miller A. Diagnosis of multiple sclerosis. In: Tselis AC, editor; Booss J, editor. Handbook of clinical neurology. Amsterdam: Elsevier BV; 2014. pp. 307–12. [Google Scholar]
22.Perry M. Swain S. Kemmis-Betty S. Cooper P. Multiple sclerosis: summary of NICE guidance. BMJ. 2014;349:g5701. [PubMed] [Google Scholar
23.Filippi M., Bar-Or A., Piehl F., Preziosa P., Solari A., Vukusic S., Rocca M.A. Multiple sclerosis. Nat. Rev. Dis. Prim. 2018;4:43. doi: 10.1038/s41572-018-0041-4. [PubMed] [CrossRef] [Google Scholar
24.Fu J., Huang Y., Bao T., Liu C., Liu X., Chen X. The role of Th17 cells/IL-17A in AD, PD, ALS and the strategic therapy targeting on IL-17A. J. Neuroinflamm. 2022;19:98. doi: 10.1186/s12974-022-02446-6. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
25.Liang H.-Y., Chen Y., Wei X., Ma G.-G., Ding J., Lu C., Zhou R.-P., Hu W. Immunomodulatory functions of TRPM7 and its implications in autoimmune diseases. Immunology. 2022;165:3–21.
26.Kamermans A., Planting K.E., Jalink K., van Horssen J., de Vries H.E. Reactive astrocytes in multiple sclerosis impair neuronal outgrowth through TRPM7-mediated chondroitin sulfate proteoglycan production. Glia. 2019;67:68–77.
27.Rossier P., van Erven S., Wade D.T. The effect of magnesium oral therapy on spasticity in a patient with multiple sclerosis. Eur. J. Neurol. 2000;7:741–744. doi: 10.1046/j.1468-1331.2000.00142.x. [PubMed] [CrossRef] [Google Scholar]
28.Cheung M.M., Dall R.D., Shewokis P.A., Altasan A., Volpe S.L., Amori R., Singh H., Sukumar D. The effect of combined magnesium and vitamin D supplementation on vitamin D status, systemic inflammation, and blood pressure: A randomized double-blinded controlled trial. Nutrition. 2022;99–100:111674.
29.P Goldberg, M C Fleming, E H Picard. Multiple sclerosis: decreased relapse rate through dietary supplementation with calcium, magnesium and vitamin D. Med Hypotheses. 1986 Oct;21(2):193-200.
30.Karpińska E., Socha K., Soroczyńska J., Kochanowicz J., Jakoniuk M., Mariak Z., Borawska M.H. Concentration of magnesium in the serum and the ability status of patients with relapsing-remitting multiple sclerosis. J. Elem. 2017;22:671–679. doi: 10.5601/jelem.2016.21.4.1156. [PubMed] [CrossRef] [Google Scholar]
31.de Oliveira M., Gianeti T.M.R., da Rocha F.C.G., Lisboa-Filho P.N., Piacenti-Silva M. A preliminary study of the concentration of metallic elements in the blood of patients with multiple sclerosis as measured by ICP-MS. Sci. Rep. 2020;10:13112. doi: 10.1038/s41598-020-69979-9. [PMC free article] [PubMed] [CrossRef] [Google Scholar]
32.Nirooei E., Kashani S.M.A., Owrangi S., Malekpour F., Niknam M., Moazzen F., Nowrouzi-Sohrabi P., Farzinmehr S., Akbari H. Blood Trace Element Status in Multiple Sclerosis: a Systematic Review and Meta-analysis. Biol Trace Elem Res. 2022 Jan;200(1):13-26.